
试验设计 动物和饮食干预:选择30只10周龄的雄性Sprague Dawley(SD)大鼠,体重380-420克,所有的大鼠都被饲养在一个有12小时光照和黑暗周期的空调房间里。在所有的实验开始之前,大鼠被禁食24小时。经过一周的适应期后,大鼠被随机分为五组(n=6),饲喂标准饮食或高脂饮食:正常饮食(CON)、高脂饮食(HF)和高脂饮食喂养的大鼠用0.4 mL XOS (2 g/mL溶解于PBS)(XOS)、正长生菌株(CMCC63516,由东北制药集团沈阳第一制药有限公司分离培养,中国,Lot S10950019)以7.5×108个CFU/mL悬浮在PBS中(BL),或XOS和BL联合补充(XOS-BL)处理。对照组大鼠被喂食正常饮食;其他组被喂食高脂饮食(60%脂肪,20%蛋白质,20%碳水化合物,占总热量的百分比,H10060,北京HFK生物科学有限公司)。XOS、BL和XOS-BL组每天灌服1次0.4毫升的XOS、BL和XOS-BL,持续三周。CON组和HF组则用0.4毫升PBS灌胃。每周评估一次体重增加和其他参数。在3周后收集粪便进行16S rRNA测序。3周后,对大鼠进行安乐死以收集血液和组织。对附睾脂肪和肾周脂肪进行称重,并计算附睾脂肪和肾周脂肪与体重的比值。 生化分析:从心脏采集血样,在25℃下以3,000 rpm的速度分离出血浆,然后在-80℃下储存待用。将肝脏组织与生理盐水按1:9的比例混合并匀浆。混合物在4℃下以12,000 rpm离心10分钟,然后保留上清液用于后续分析。根据相关检测试剂盒的说明,用酶法检测血清总胆固醇(TC)、甘油三酯(TG)、高密度脂蛋白胆固醇(HDL-C)和低密度脂蛋白胆固醇(LDL-C)的浓度(南京建城生物技术研究所,中国南京)。血清和肝脏中的LPS水平用ELISA试剂盒检测(上海冷顿生物科学有限公司,中国上海)。 变性梯度凝胶电泳(DGGE):使用QIAamp DNA Stool Mini Kit(Qiagen, Hilden, Germany)提取粪便DNA。使用通用细菌引物F338+GC钳和R518进行PCR扩增,该引物针对16S rRNA基因的高变异V3区。使用Bio-Rad公司(Hercules, CA, USA)的DCode系统对所得的16S rDNA扩增子进行DGGE指纹分析;用Quantity One图像分析软件(4.6.1版;Bio-Rad)对DGGE图像进行分析。相似性以树状图的形式显示。 Illumina HiSeq测序和生物信息学分析:使用通用引物(520F,802R)扩增五组大鼠粪便中元基因组DNA的16S核糖体DNA的V3-V4区(每组n=5-6)。PCR产物经1.5%(w/v)琼脂糖凝胶电泳在0.5 mg/mL溴化乙锭中检查并纯化。在Novogene(中国北京)的Illumina HiSeq平台上进行测序。在50%以上的粪便样本中出现的操作分类单位(OTU)被确定为核心OTU。根据OTU的结果,对α和β多样性进行分析。α多样性由观察到的物种和香农指数进行评估。群落丰富度由Chao1指数评估。β多样性通过主坐标分析(PCoA)评估,基于加权的UniFrac分析和非加权对群法与算术平均聚类(UPGMA)。线性判别分析效应大小(LEfSe)被用来识别不同分类水平的组间有差异的细菌类群。线性判别分析(LDA)被用来估计每个不同丰度特征的效果大小。 试验结果 (1)BL联合XOS对HFD喂养大鼠体重、脂质参数和炎症标志物的影响 如图1(a)和1(b)所示,与对照组相比,HFD在第6天后诱导了最终体重和体重增加的显著升高(P<0.0001);图1(b)显示,BL和XOS的联合补充(XOS-BL)降低了这种增加的趋势(P=0.0588),3周后,联合补充BL和XOS显著降低了HFD喂养大鼠的体重增加(P=0.0323);然而,图1(c)和1(d)显示,各组之间在附睾和肾周脂肪垫的总重量上无显著差异;图2(a)和2(c)显示,与HF组相比,XOS-BL组的血清TC和LDL-C水平显著下降(分别为P=0.0027和P<0.0001);图2(b)和2(d)显示,与HF组相比,XOS-BL组的TG水平呈下降趋势,而HDL-C水平呈上升趋势;此外,还评估了BL和XOS对肥胖大鼠的抗炎能力;图2(e)显示,与HF组相比,我们观察到XOS-BL组的血清LPS水平显著下降,表明内毒素血症和系统性慢性炎症的缓解(P=0.0346);在BL和/或XOS处理后,还对大鼠肝脏的LPS水平进行了评估;图2(f)显示,与HF组相比,BL组的肝脏LPS显著降低(P=0.049)。这些结果说明,联合补充BL和益生元XOS可以有效地改善肥胖大鼠的体重和血清参数。
(2)联合BL和XOS对HFD大鼠肠道菌群的影响 如图3(a)所示,对照组和HF组大鼠肠道微生物丰度有显著差异;基于DGGE图谱构建的树状图支持它们加入到不同的聚类;图3(b)显示,HF组和BL组在一起,而XOS组和XOS-BL组在一个簇中;在图3(a)中,选择了23条在各组间有明显差异的条带,并将其切除进行测序分析;为验证DGGE的分辨能力,对相同位置但不同通道的条带进行切割和测序。测序结果表明,它们属于同一菌群,汇总于表1。CON组的微生物群的特点是存在乳酸菌属(条带1和3);Phascolarctobacterium succinatutens(条带5)和Bacteroides uniformis(条带6和7)在高脂饮食组中被确认;XOS和XOS-BL组表现出与P. succinatutens相对应的强烈条带;在CON、XOS和XOS-BL组中分别检测到与Prevotella copri(条带2和11)相对应的条带;XOS和BL组的模式显示了对应于Parabacteroides distasonis的条带,特别的是,在XOS组中发现了对应于假长双歧杆菌的条带23。
如图4所示,对16S rRNA基因序列的V3-V4区进行宏基因组分析,在抽样后,1,124个操作分类单位(OTU)以97%的相似度被分类;图4(a)显示,对照组的OTU数量为908,远远高于其他组,其中,对照组有156个OTU,HF组有39个OTU,而XOS组、BL组和XOS-BL组分别有14个、22个和18个OTU;图4(b)-4(d)显示,α多样性分析显著,各组间差异显著,表明高脂饮食及给予BL和XOS显著改变了肠道菌群的多样性和丰富度;图4(e)和4(f)显示,各组肠道微生物群组成存在明显的聚类(对照组与HF,R=0.615,P=0.001;HF与XOS,R=0.441,P=0.001;HF与BL,R=0.075,P=0.606;HF与XOS-BL,R=0.454,P=0.001),表明XOS-BL的摄入方式对HFD喂养大鼠的肠道微生物群组成有一定影响。 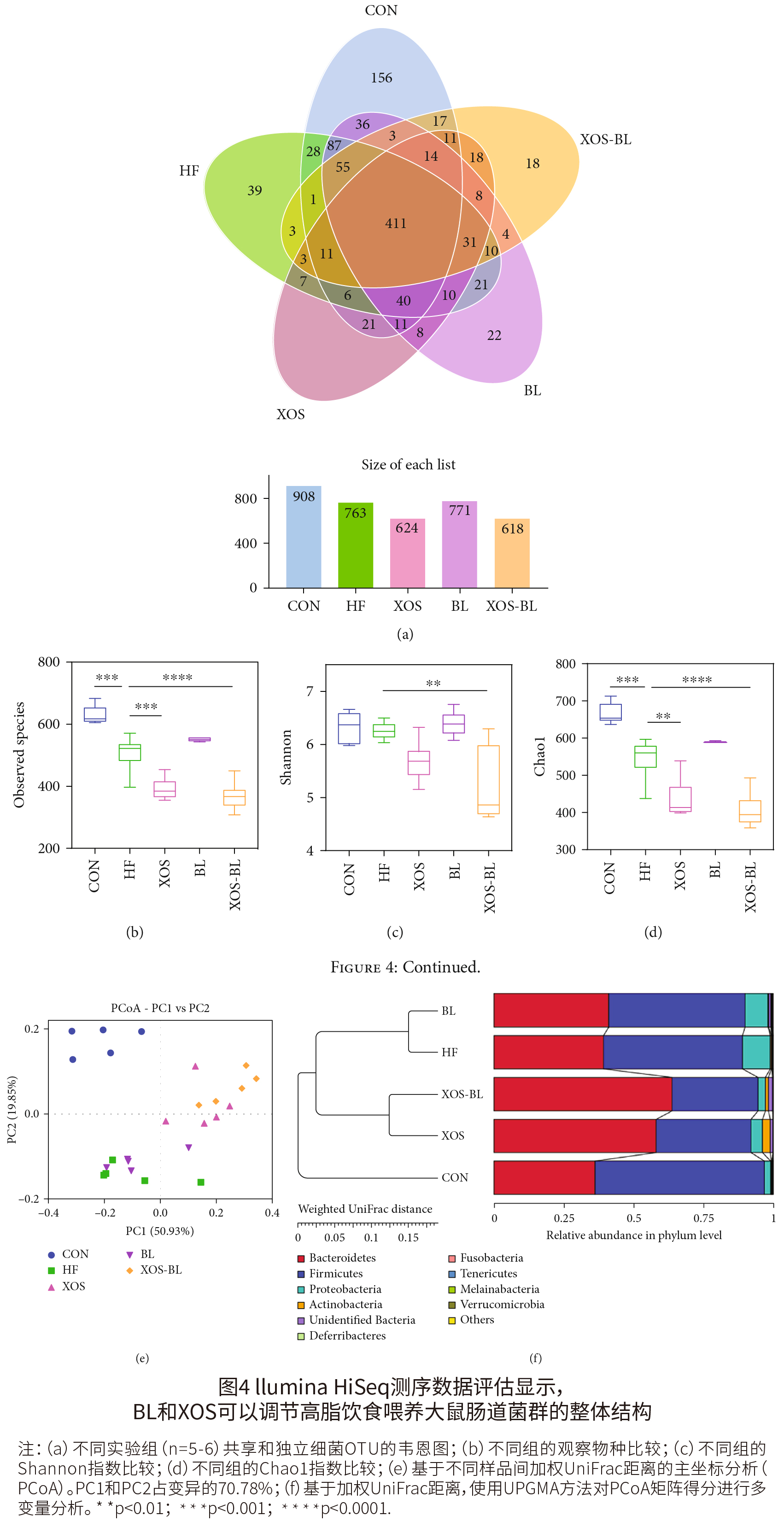 如图5(a)所示,本研究中SD大鼠粪便菌群主要有三个门:拟杆菌门、厚壁菌门和变形菌门;厚壁菌门与拟杆菌门的比值(F/B),广泛用于肠道生态失调的标志,图5(b)显示,与HF组相比,XOS-BL组的F/B值显著较低(P<0.01)。我们的研究结果表明,导致厚壁菌门和拟杆菌门变化的主要分类群是拟杆菌属和乳酸菌属。与HFD组相比,CON组大鼠的总乳酸杆菌丰度显著较高(+19.7%,P<0.01);图5(c)显示,在XOS-BL组中,普雷沃特氏菌科和粪拟杆菌的丰度不同(P<0.01);图5(d)和5(e)显示,产生SCFA的Parabacteroides属(拟杆菌的成员)和Blautia属(厚壁菌门的成员)是XOS组小鼠的关键分类群,进一步检验科、属和种层面的统计学差异;图6(a)显示,在科水平上,在XOS和BL的补充下,Prevotellaceae显著升高,而Ruminococcaceae、Desulfovibrionaceae和未识别的梭菌科(Clostridiales)显著减少;图6(b)显示,在属水平上,XOS和BL处理改变了3个代表性属。在XOS和BL处理后,厌氧菌显著增加,而未识别的梭菌和Tyzzerella显著减少;图6(c)显示,在物种水平上,有2个物种被XOS和BL处理改变,XOS联合BL干预均能显著降低单形拟杆菌和细菌YE57。
(3)各组生物标记物 如图7所示,采用宏基因组分析LEfSe方法确定了导致类群差异的关键系统类型。LDA评分图显示了各组中的优势细菌(LDA>4);乳酸菌科在对照组大鼠中最多,而 Desulfovibrionaceae,Rikenellaceae和 Ruminococcaceae在HFD喂养大鼠中最多。在XOS处理的大鼠中,双歧杆菌科和Erysipelotrichaceae最为丰富;在BL处理的大鼠中,拟杆菌科最为丰富;而在XOS+BL处理的大鼠中,普雷沃氏菌科最为丰富。这些细菌是造成不同组的肠道微生物群差异的主要系统类型,此外,这一结果与图3和表1中DGGE的结果一致。
(4)LPS水平与微生物类群的关系 如图8(a)所示,Mantel检验和典型相关分析(CCA)表明,血清和肝脏的LPS水平是造成细菌群落和环境因素之间差异的主要因素(P=0.005);图8(b)显示,本研究通过Spearman算法评估了肠道微生物群组成和LPS水平之间的相关性,一些肠道微生物的丰度,包括乳酸杆菌、未识别的Ruminococcaceae,Roseburia和Butyrivibrio与血清和肝脏的LPS水平呈正相关;相比之下,Blautia,Flavonifractor,双歧杆菌, Parabacteroides,Lachnoclostridium,Erysipelatoclostridium和Staphylococcus与血清和肝脏LPS水平呈负相关。
试验结论 本研究表明,联合补充BL和XOS可以抑制高脂饮食引起的F/B比值的上升,以及Desulfovibrionaceae和Ruminococcaceae丰度的升高和LPS水平的升高。这些结果表明,将地衣芽孢杆菌和益生元XOS结合起来作为一种饮食干预策略,可以改善肠道失调,改善炎症状态,从而减少与HFD诱导的肥胖相关疾病。 参考资料: Yuyuan L ,Man L ,He L , et al.Oral Supplements of Combined Bacillus licheniformis Zhengchangsheng® and Xylooligosaccharides Improve High-Fat Diet-Induced Obesity and Modulate the Gut Microbiota in Rats.[J].BioMed research international,2020,20209067821. |